Enthalpie
Die spezifische Enthalpie h [kJ/kg] stellt die gesamte im Dampf enthaltene Wärmemenge dar.
Die Enthalpie teilt sich dabei in den fühlbaren Anteil, bei dem eine Temperaturänderung stattfindet, und den latenten („verborgenen“) Anteil auf, bei dem bei konstanter Temperatur der Anteil des Dampfs zwischen 0 ... 100 % variiert.
Beim Aufheizen findet bis zum Erreichen der Siedelinie eine Erwärmung des Wassers statt. Wird die Siedelinie erreicht, steigt bei weiterer Energiezufuhr der dampfförmige Anteil, bis das Wasser vollständig verdampft ist.
Die spezifische Verdampfungsenthalpie r von Wasser in [kJ/kg] ist diejenige Wärmemenge, die 1 kg Wasser zugeführt werden muss, um vom flüssigen in den dampfförmigen Zustand zu gelangen. Da die Wärmezufuhr im Kessel bei konstantem Druck stattfindet und daher auch keine Temperaturerhöhung erfolgt, wird diese Wärmemenge auch als latente = „verborgene“ Wärme bezeichnet.
Umgekehrt findet der gleiche Vorgang bei der Abgabe von Wärme statt. Zunächst wird der Dampf durch die Abgabe der latenten Wärme an das Produkt kondensiert, bis nur noch flüssiges Wasser vorliegt. Erst dann findet eine Abkühlung des Kondensats statt. Diese Abkühlung im Kondensat wird häufig auch als Unterkühlung unter die dem Dampfdruck zugehörige Temperatur der Siedelinie bezeichnet.

|
Fühlbare Wärme Latente Wärme |
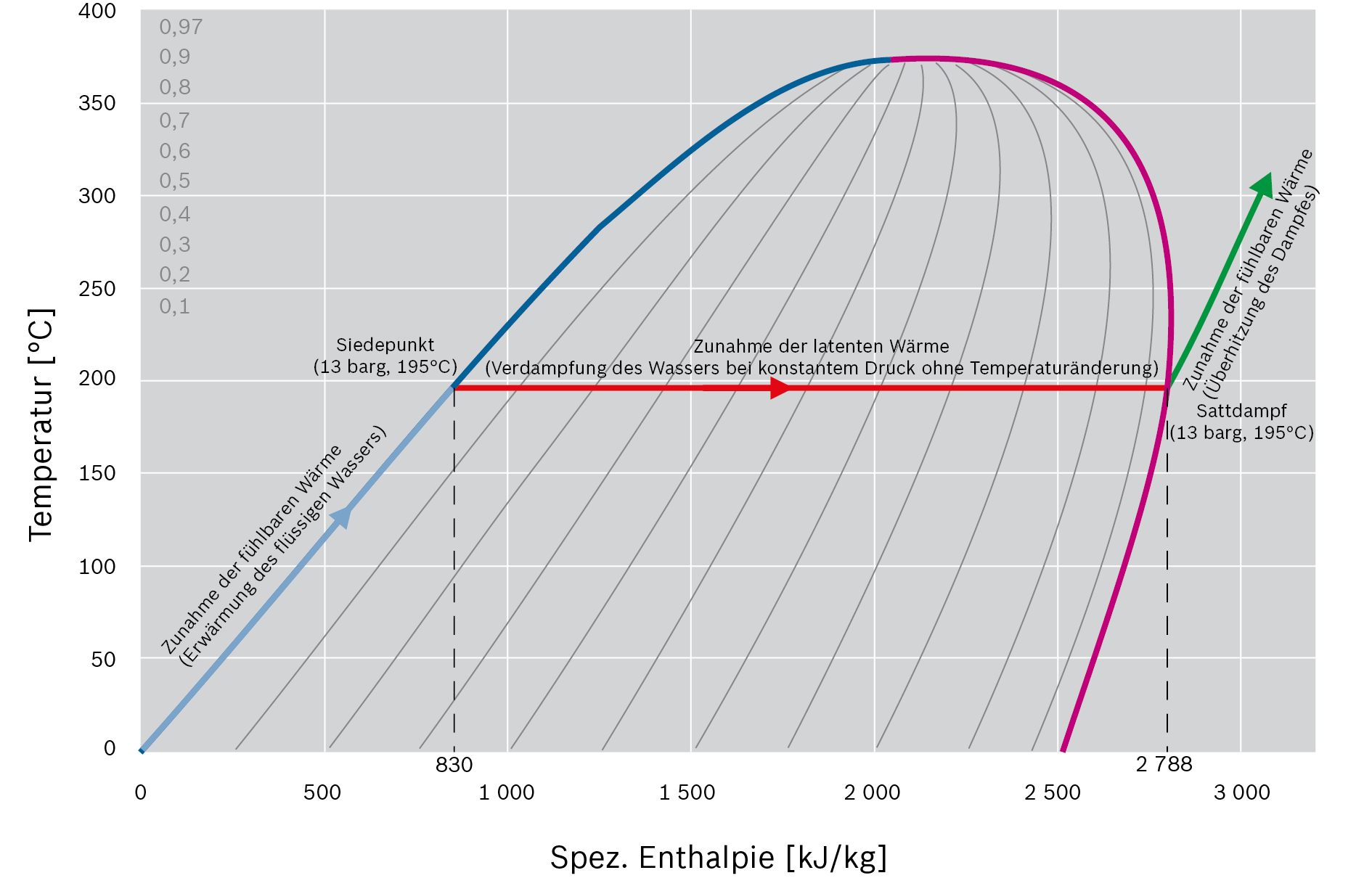
Konzept der fühlbaren und latenten Wärme im Temperatur-Enthalpie-Diagramm (T-h-Diagramm)
|
|
Gesättigte Flüssigkeit |
|
Druckwasser |
|
Überhitzter Dampf |
||
|
|
Sattdampf |
|
Nassdampf |




